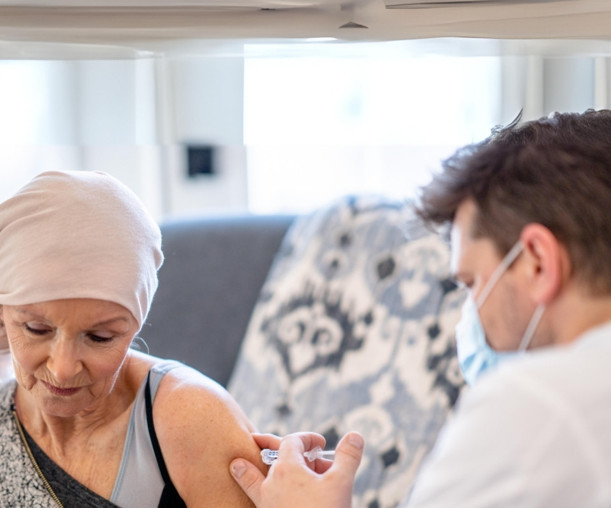
BioNTech’in akciğer kanseri aşısı bir yıldır Türkiye’de bulunan beş hastanede deneniyor
BioNTech, dünyanın ilk mRNA akciğer kanseri aşısını denemeye başladı. 7 ülkede 34 merkezde başlayan çalışmaların bir ayağı da Türkiye’de bulunan beş hastanede sürüyor.
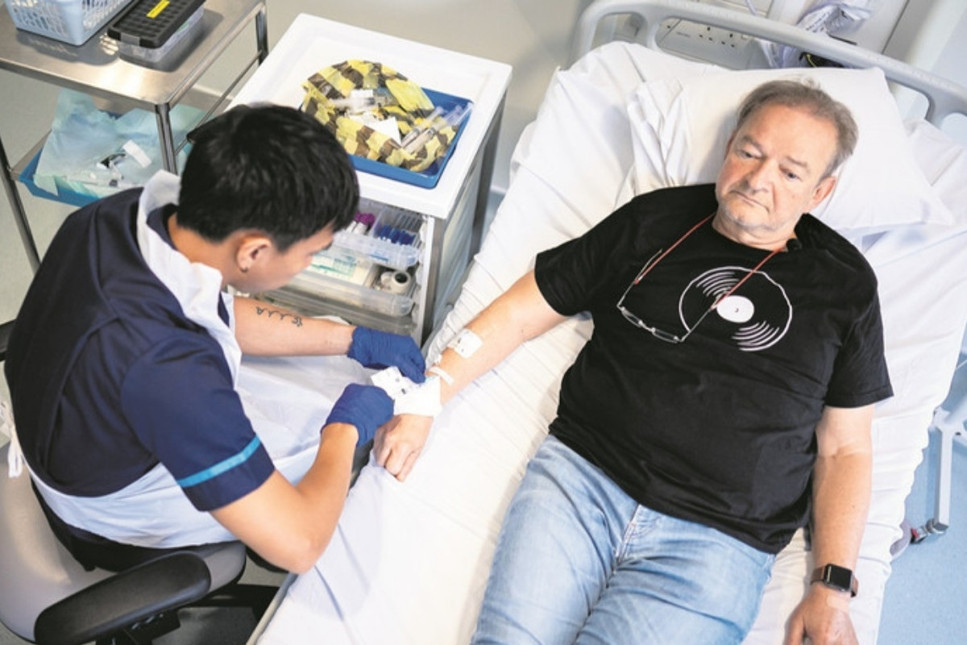
Türkiye’deki araştırmalar yaklaşık bir yıldır devam ediyor ve elde edilen sonuçlar 7-10 Eylül tarihlerinde ABD’de toplanacak kanser konferansında dünyayla paylaşılacak.
Prof. Dr. Uğur Şahin, 9 Kasım 2020’de “Bu; ilerleme, bilim ve global işbirliği adına kazanılmış bir zafer” sözleriyle BioNTech ve Pfizer ortaklığıyla geliştirilen Covid-19 aşısının yüzde 90’dan fazla etkinlik sağladığını açıkladı. Aynı yılın 11 Mart günü Dünya Sağlık Örgütü (DSÖ) “küresel salgın” alarmı vermiş, dünya mRNA aşısı geliştirilene kadar geçen yedi ay boyunca amansız bir salgınla yüzleşmek zorunda kalmıştı.
Oksijen,'den Baran Can Sayın'ın haberine göre, aşı 7 ay gibi rekor bir sürede ortaya çıktı, çünkü BioNTech, 2008’den beri mRNA teknolojisi üzerinde çalışıyordu. Prof. Dr. Uğur Şahin, doktora derecesini 1993’te Köln Üniversitesi’nden ‘tümör hücrelerinde immünoterapi’ üzerine yaptığı çalışmayla almıştı. Aklında ve araştırmalarının odağında daima kanseri, enfeksiyon hastalıklarını, bağışıklık ve sinir sistemi rahatsızlıklarını immünoterapiyle çözmek vardı.
İngiltere’de aşıyı yaptıran ilk kişi 67 yaşındaki Janusz Racz oldu. Mayısta kanser teşhisi konulan ve kısa sürede kemoterapi ve radyoterapi almaya başlayan Racz “Benim için çok faydalı olacak çünkü diğer hastalarda uygulanmayan yeni bir yöntem” dedi.
KANSERE ÇARE HAYALİ
2002’de evleneceği Dr. Özlem Türeci de aynı düşün peşindeydi; öyle ki, nikah törenlerinden sonra çalışmak için doğruca laboratuvara dönmüşlerdi. Çift, moleküler biyoloji alanında saygın bilim dergisi EMBO’ya 2021’de şunları söyleyecekti: “2001’de Ganymed’i kurarken de, 2008’de BioNTech’i kurarken de aklımızda kanser hastalarını iyileştirebilmek vardı. Fakat tedavinin en çetin yanı, her hastanın farklı bir tümöre sahip olması. Kanser tedavilerinin başarısızlığının altında yatan neden de bu. Çözüm bize göre kişiselleştirilmiş tıptan geçiyor. BioNTech’i bu yüzden kurduk. mRNA hep odak noktalarımızdan biriydi. 20 yılı aşkın bir süre boyunca kullanılabilmesi için üzerinde çalıştık.”
2026’DA PİYASADA OLABİLİR
İlk mRNA kanser aşısının denemelerine 2014’te başladılar. Pandemi patlak verdiğinde onlar hala mRNA teknolojisini kullanıp kanserli hücreleri bağışıklık sistemine tanıtarak vücudun kansere karşı antikor üretmesini sağlamaya çalışıyorlardı. Covid-19’la mücadele için de bu teknolojinin uygulanabileceğini fark ettiler. Ürettikleri aşı pandeminin seyrini değiştirdi, tüm dünyada 13.6 milyar doz aşı uygulandı. Küresel acil durumun sona erdiği DSÖ tarafından geçen yılın mayıs ayında duyurulunca şirket, ana odağına döndü.
Önce geçen kasımda Prof. Şahin, Alman Bild am Sonntag’a verdiği demeçte mRNA tabanlı ilk kanser aşılarının 2030 olmadan onay almasını beklediğini belirtti. Şubat ayında ise Prof. Şahin ile Dr. Özlem Türeci, Focus dergisine verdikleri röportajda “30 tür kansere karşı klinik araştırmalarını sürdürdüklerini, bu çalışmalardan 10’unun ruhsat almaya yakın olduğunu ve 2026 itibarıyla kanser aşılarını piyasaya sürmeyi öngördüklerini” söylediler.
KANSER TEDAVİSİNDE MRNA TEKNOLOJİSİ
İşte Şahin ve Türeci’nin bahsettiği bu aşılardan biri mRNA ile akciğer kanseri tümörünün genetik kodlarını vücuda tanıtarak kanserli hücrelerin alt edilmesini amaçlayan BNT116. Aşıyla alakalı son gelişme İngiliz yayın organı Guardian’da yayımlandı. 23 Ağustos tarihli habere göre Faz-1 aşamasında olan BNT116’nın İngiltere’de uygulandığı ilk kişi, 67 yaşındaki Janusz Racz oldu. Aşı çalışmaları yalnız İngiltere’de değil, Türkiye, ABD, Almanya, İspanya, Macaristan ve Polonya olmak üzere 7 ülkede 34 merkezde yürütülüyor.
BNT116 Türkiye’de Ankara Dr. Abdurrahman Yurtaslan Onkoloji Eğitim ve Araştırma Hastanesi, Ankara Bilkent Şehir Hastanesi, Yeditepe Üniversitesi Hastanesi, Ege Üniversitesi Tıp Fakültesi Tülay Aktaş Onkoloji Hastanesi ve Dokuz Eylül Üniversitesi Hastanesi’nde deneniyor.
BNT116 üzerine çalışan merkezlerden Ege Üniversitesi Tıp Fakültesi’nden Prof. Dr. Erdem Göker ile Ankara Bilkent Şehir Hastanesi’nden Prof. Dr. Mehmet Ali Nahit Şendur yapılan araştırma, izlenen yöntem ve süreç ile ilgili Oksijen’in sorularını yanıtladı.
“BİZ İNGİLTERE’DEN BİR YIL ÖNCE BAŞLADIK”
Ege Üniversitesi Tıp Fakültesi’nden Prof. Dr. Erdem Göker, İngiltere’de çalışma yeni başladığı için geçen hafta dünya gündemine geldiğini söylüyor: “Araştırma bizde yaklaşık bir yıldır sürüyor. Gönüllü alımına halen devam ediyoruz. Unutulmamalı ki bu koruma değil, tedavi aşısı. Türkiye’de aşıların Faz-1 araştırmalarının yapılması için gerekli Sağlık Bakanlığı akreditasyonuna sahip 7 merkezden 5’inde bu araştırma yürütülüyor. BioNTech özelinde şöyle bir durum da var: Uğur Şahin ve Özlem Türeci, Türkiye’yi öncelikli ülkeler arasında görüyor.”
“HASTANIN MASRAFLARINI BİONTECH KARŞILIYOR”
“Şirketler önce projeyle akredite kurumlara başvuruyor. Kurum iç onay verirse teklif Sağlık Bakanlığı’na taşınıyor ve bakanlığın onayı da gerekiyor. Bunlar en az 4-6 ay sürüyor. Onaylandığında kurumun uzmanları kriterlere uygun gördüğü hastalara projeden bahsediyor. Bir dosya şeklinde sunulan ve aşının özellikleri, yan etkileri gibi tüm unsurlarına değinen gönüllü olma formunu okuyup kabul ederlerse çalışmaya katılıyorlar. Hastaların sağlık masraflarını, şehir dışından geliyorsa yol harcamasını şirket karşılıyor. Hasta kontrolü, tedavisi ve diğer tüm çalışmaları hastane ekibi olarak biz yürütüyoruz. Şirket yalnızca ilaç temin ediyor. Sağlık harcamalarına sponsorluk yapıyor ve bilgi topluyor. Başka bir müdahalesi yok.”
EYLÜLDE ABD’DE AÇIKLANACAK
“Bu tüm araştırmalarda geçerli prosedür. BNT116’da Faz-1 aşamasındayız. Faz-1 az sayıda gönüllüyle yürütülür ve ilacın güvenli olup olmadığına bakılır. Yan etkileri ve toksisitesi saptanır. Veriler yeterli ve sağlıklı bulunduğu takdirde Faz-2 aşamasına, bazen doğrudan Faz-3 aşamasına geçilir. İlacın etkinliğinin incelendiği ve gönüllü sayısının arttırıldığı aşama Faz-2’dir. Faz-3’te ise binlerce gönüllüden data toplanır ve sonuçlar olumluysa ruhsat alınıp üretime geçilir.
Aşının etkinliği konusunda henüz ön bulgulara sahibiz. Kesin konuşmak mümkün olmasa da izlenimim olumlu yönde. Ama kanıtlanması gereken çok şey var. 7-10 Eylül arası San Diego’da Dünya Akciğer Kanseri Konferansı’nda bir ön rapor açıklanacak.”
“KLİNİK ARAŞTIRMALAR TÜRKİYE İÇİN BİR ŞANS”
“Bu deneklik değil. Kamuoyuna maalesef böyle yansıtılıyor. Oysa bu tür klinik araştırmalar çok büyük bir şans. Ülkemizde uygulanması da insanlarımız için çok olumlu. Şirket, hastane ve gönüllüler arasında ekonomik bir çıkar ilişkisi yok. Hastalarımız bu sayede normal şartlarda ulaşamayacakları ilaçlara erişiyor. Araştırmalara katılım arttıkça ilaçların geliştirilme süresi de kısalıyor. Çünkü bir kanser ilacının geliştirilmesi ortalama 10 yılı buluyor.”
“ŞİMDİLİK YAN ETKİLERİ GÖZLÜYORUZ”
Ankara Bilkent Şehir Hastanesi’nden Prof. Dr. Mehmet Ali Nahit Şendur ise şunları söylüyor:
“Şu aşamada yan etkileri gözlemek adına standart tedavileri tüketmiş hastaları seçiyoruz ve kemoterapi ya da başka ilaçlarla tedaviyi kombine ederek çalışmayı yürütüyoruz. Gözlemlerimize göre yüzde 15-20 oranında tümör yanıtı veriyor. Ne kadarı aşıdan, ne kadarı destekleyici tedavilerden kaynaklı, henüz saptanmadı. Güvenli olup olmadığını tespit edersek ve onay da alınırsa etkinliğini inceleme safhasına geçeceğiz.”
GÖNÜLLÜLÜK KRİTERLERİ
“Toplam kaç gönüllünün olduğunu bilmiyorum ama muhtemelen 100’ün üzerinde. Şirketin Faz-1 hedefi 130 gönüllü. Bu sayı sonuçlara göre güncellenebilir de. Hastanemizde 8 hasta katıldı. Tüm akciğer kanseri hastalarını dahil etmiyoruz. İlk olarak hastanın genel durumunun tedavi kaldırır durumda olması gerek.
Kanser türünün küçük hücreli dışı akciğer kanseri olması da diğer şart. Akciğer kanserine yakalananların yüzde 85’i bundan muzdarip. Aşıyı hastalığı 3 ve 4’üncü evrede bulunan, standart tedavileri tüketmiş hastalarda denedik.”
“HENÜZ KANITLANMADI, MUCİZEVİ BİR ÇÖZÜM YOK”
“Henüz kesin olarak kanıtlanmış bir şey yok elimizde. Buna mucizevi bir çözüm, yeni bir teknoloji olarak bakılmasın. Faz-1’de uygun doz saptanır. Aşının mevcut tedavi yöntemleriyle aynı veya onlardan daha fazla etkinlik sağladığı görülürse Faz-2’ye geçilir ve daha fazla gönüllü alınır. Faz-1’in doğası gereği bu araştırmaya katılan merkezler sınırlı bir gönüllü havuzuyla ilerlemek durumunda. Akciğer kanseri olan insanların çok az bir kısmı araştırma kriterlerini sağlıyor. Bir yıldan beri kliniğimizdeki yüzlerce hastadan ancak 8’i bu şartları karşıladı.”
Gönüllü olabilmek için gereken diğer kriterler, Clinical Traits’teki çalışma kaydında şöyle sıralanıyor:
- Gönüllülerin ilerlemiş ya da metastatik küçük hücreli dışı akciğer kanserine sahip ve radyoterapi sonrası tümörü alınamayacak durumda olması gerekiyor.
- Tüm tedavi metotlarının denenmiş ya da uygulanamayacak vaziyette olması şart.
- Aktif tedavi alan hastalar araştırma için gönüllü olamıyor.
- Önemli bir otoimmün hastalığa sahip olanlar araştırma kapsamına dahil edilmiyor.
patronlardunyasi.com